NORMAS DE DIAGNOSTICO Y TRATAMIENTO DE LA HIDATIDOSIS HUMANA
PROVINCIA DE RIO NEGRO (ARGENTINA)
RESOLUCION 3720/2002. SECRETARIA DE ESTADO DE SALUD
Grupo de Elaboración y Redacción:
Por orden alfabético:
Dr. Mario Del Carpio (Médico Cirujano), Hopital R. Cortizo, Ing. Jacobacci
Dr. Antonio Gatti (Bioquimico), Hospital A. Zatti, Viedma.
Dr. Carlos Hugo Mercapide (Jefe de Servicio Cirugía), Hospital A. Zatti, Viedma.
Dr. Martín Odriozola (Jefe de Servicio Cirugía), Hospital R. Carrillo, Bariloche.
Dr. Hector Panomarenko (Médico Generalista), Hospital de Area, El Bolsón
Dr. Rubén Pereyra (Médico Cirujano), Hospital A. Zatti, Viedma.
Dr. Alicia Perez(Bioquimica). Laboratorio de Zoonosis, Bariloche
Dr. Juan Carlos Salvitti (Médico Cirujano), Hospital Carrillo, Bariloche
Dr. José Sustersic (Médico Cirujano), Hospital Lopez Lima, Roca.
.
Asistencia Técnica (Médicos Veterinarios)
Dra. María Teresa Costa, Unidad Regional Epidemiología, Jacobacci
Dr. Gustavo Cantoni, Unidad Regional Epidemiología, Bariloche
Dr. Jose Labanchi, Unidad Regional Epidemiología, Roca
Dr. Sergio Mancini, Unidad Regional Epidemiología, Viedma
Dr. Ricardo Bigatti, Programa de Control de Hidatidosis, Secretaría de Salud
Coordinación General
Dr. Edmundo Larrieu(Médico Veterinario), Dirección Areas Prioritarias, Secretaría de Estado de SaludANEXO I
NORMAS DE DIAGNÓSTICO Y TRATAMIENTO
DE LA HIDATIDOSIS HUMANA
INTRODUCCION: BASES EPIDEMIOLOGICAS PARA EL DIAGNOSTICO Y EL TRATAMIENTO DE LA HIDATIDOSIS HUMANA
El Echinococcus granulosus en su forma adulta vive en el intestino del perro, eliminando huevos periódicamente con la materia fecal. Estos huevos pueden ser ingeridos accidentalmente por los huéspedes intermediarios, entre ellos el hombre. Los huevos eclosionan, liberando el embrión hexacanto en el intestino delgado. Este, a través de las vellosidades intestinales pasa a la circulación venosa hasta alojarse en el tejido hepático donde formará la hidátide. A las 72 horas de la ingestión del huevo, la larva alcanza un tamaño de 20 micrones, mientras que a los 7 días puede identificarse una formación esférica y francamente hidatídica.
En caso de ser superado el filtro hepático el embrión continúa por el sistema circulatorio hasta el pulmón. Eventualmente puede continuar su migración alcanzando variadas localizaciones tal como riñón, cerebro, tejido óseo, muscular, etc.
El crecimiento del parásito dependerá del potencial evolutivo del embrión hexacanto, del tejido circundante y de la resistencia del huésped.
Así, el pulmón, de características elásticas, ofrece una escasa resistencia a su crecimiento. Ello determina un aumento de tamaño proporcionalmente rápido llevando a la aparición de síntomas clínicos en un gran porcentaje de los casos.
En el hígado, por su parte, la resistencia del tejido circundante es fuerte lo que determina que en muchos casos el crecimiento sea lento o incluso nulo durante muchos años, permitiendo que un alto porcentaje de portadores permanezca sin síntomas clínicos durante toda su vida.
Estos aspectos se traducen en una relación entre las localizaciones hígado/pulmón 2/1 a 3/1 en los servicios hospitalarios que reciben pacientes con síntomas clínicos. Las restantes localizaciones usualmente no superan el 10% de los casos detectados. Estos coeficientes expresan la importancia del filtro hepático como elemento determinante para la localización del quiste.
Los estudios en autopsias, por su parte, muestran una relación entre las localizaciones hepática y pulmonar de 4/1 y en donde entre el 63,3 % y el 84,5 % de los casos resultan de hallazgos sin relación alguna con la causa de muerte. Esta cifra refuerza el criterio del filtro hepático como factor primordial para determinar localización y expresa que un porcentaje importante de los quistes hepáticos no alcanza a producir enfermedad en el huésped, manteniéndose un estado de equilibrio agente/huésped durante toda la vida.
1- DIAGNOSTICO DE LA HIDATIDOSIS EN EL HOMBRE:
1.1.- DIAGNOSTICO POR IMÁGENES:
1.1.1.- HIDATIDOSIS HEPATICA Y ABDOMINAL: Se debe considerar a la Ecografía como técnica de elección para:
a- Diagnóstico en pacientes sintomáticos.
b- Control del tratamiento
c- Encuestas de población para detección de portadores no sintomáticos a localización abdominal (90% de los quistes hidatidicos). En estos casos la Sensibilidad de la técnica es del 100% y del 96% la Especificidad.
d- Vigilancia epidemiológica.
Desde el punto de vista de las imágenes ultrasonográficas del quiste hidatídico, se han definido varias características patognomónicas:
a.- vesículas aisladas.
b.- vesículas hijas múltiples.
c.- observación del "nevado" dado por la movilización de la arenilla hidatídica al movilizar bruscamente al paciente 180 grados.
d.- aparición de membranas desprendidas.
e.- pared del quiste hidatídico de mayor espesor (diferencia con quistes serosos simples o de enfermedad poliquística).
Los diagnósticos ultrasonográficos deberán incluir la clasificación de Gharby (tipo de quiste):
TIPO I : Hialino
TIPO II : Membranas “plegadas”
TIPO III : Con Vesículas Hijas
TIPO IV : Sólido Heterogéneo
TIPO V : Calcificado
En todos los casos se incluirá la correcta medición del tamaño y ubicación ecográfica del quiste, elementos indispensables para la decisión terapéutica y para el control y seguimiento de los pacientes.
Los demás métodos de diagnósticos por imágenes (TAC – RMN) se reservan para casos seleccionados y/o con Ecografía dudosa.
Las residencias en Medicina General deberán incluir entrenamiento en ecografía de campo en su curriculum.
1.1.2.- HIDATIDOSIS PULMONAR: Se debe considerar a la radiografía de tórax (frente y perfil): como técnica de elección para:
a- Diagnóstico en pacientes sintomáticos
b- Control del tratamiento
c- Encuestas de población para detección de portadores no sintomáticos a localización pulmonar (10% de los quistes hidatidicos).
1.2.- DIAGNOSTICO DE LABORATORIO:
1.2.1.- ELISA (anticuerpos): Util como técnica tamiz en encuestas para detección de poblado-res no sintomáticos, particularmente en ausencia de tecnología ecográfica.
1.2.2.- ELISA (antígeno circulante): ó Elisa de captura. Util para el seguimiento de pacientes operados y/o en tratamiento con Albendazol. La primer determinación debe realizarse antes de la cirugía o de iniciarse el tratamiento.
Se deben realizan controles a los 10 y 30 días de la cirugía, a los 3 meses y después cada 6 meses. Normalmente a los 30 días se negativiza.
En el caso de los pacientes bajo tratamiento médico, se deben realizan las determinaciones cada 3-6 meses.
En pacientes sintomáticos, con hidatidosis confirmada quirúrgicamente, se ha reportado que el 80% de los casos presentan serología positiva para hemaglutinación indirecta, 82% a 88% para doble difusión cinco, 82% para inmunoelectroforésis, 88% a 96% para enzimoinmunoensayo, y 92% para inmunoblot. La especificidad de estos métodos varía del 95% del HAI al 100% del DD5.
En portadores sin síntomas clínicos la información es muy limitada, aunque la respuesta serológica es marcadamente menor.
Por ejemplo, la sensibilidad y especificidad de las pruebas de doble difusión cinco y del enzimoinmunoensayo han sido estimadas en la Provincia de Río Negro utilizando estudios completos por imágenes (radiología, ultrasonografía y tomografía) como pruebas de referencia, resultando del 63% y 97.05% respectivamente para Enzimoinmunoensayo a títulos iguales o superiores a 8 DE, y 31% y 100% respectivamente para DD5. En función de ello:
- DD5: No se recomienda su uso, por baja sensibilidad y elevado consumo de antígeno.
- HAI: No se recomienda su uso, por presentar falsos positivos y falsos negativos. Su sensibilidad y especificidad son menores al ELISA.
En todos los casos la negatividad de una prueba serológica no puede descartar la presencia de un quiste hidatídico, tanto en portadores sanos como pacientes sintomáticos.
1.3.- ENCUESTAS DE POBLACION
Su bajo costo operativo, rapidez de obtención de resultados, alto rendimiento diagnóstico y precisión del resultado (valor predictivo positivo actual en la Provincia de Río Negro 20%, valor predictivo negativo 100%) colocan a la encuesta ultrasonográfica como método de elección en el diagnóstico precoz de la hidatidosis humana en áreas endémicas.
Sin embargo, y de no disponerse de equipamiento ultrasonográfico para su utilización sistemática en ambientes rurales endémicos, podría ser utilizado el enzimoinmunoensayo como prueba tamiz, siendo los casos reactivos derivados a centros de mayor complejidad para ser estudiados con ultrasonografía abdominal y, eventualmente, radiología pulmonar.
2- TRATAMIENTO DE LOS QUISTES HIDATIDICOS HEPATICOS:
Las sugerencias de tratamiento que a continuación se detallan surgen de la experiencia hasta ahora acumulada en el desarrollo del programa de control y tratamiento de estos pacientes y son de orientación general, debiendo el médico tratante tener en cuenta en forma individual a cada paciente a fin de poder identificar y evaluar aquellas situaciones particulares (como ser: edad, enfermedades previas, contraindicaciones específicas, ocupación, domicilio, posibilidades de realizar los controles necesarios, etc.) que puedan hacer necesario adecuar el tratamiento a las condiciones particular del paciente. Ante cualquier duda se sugiere comunicarlas al Comité Médico Provincial y/o a sus referentes regionales.
Se deben considerar dos situaciones:
a).- Pacientes sintomáticos y/o con quistes hidatídicos complicados
b).- Portadores asintomáticos de quistes hidatídicos.
Se deben evaluar correctamente los síntomas referidos por el paciente para determinar si realmente son causados por el Quiste Hidatídico o si son originados por otra patología asociada.
A todos los pacientes se le debe realizar, además de la ultrasonografía, radiología de torax antes de decidir la conducta a seguir.
2.1.- PACIENTES SINTOMATICOS Y/O COMPLICADOS:
Ya sea por infección, ruptura a cavidad abdominal o la vía biliar, tránsito toraco-abdominal, o tumor palpable se sugiere TRATAMIENTO QUIRURGICO CONVENCIO-NAL.
En estos casos se efectuará tratamiento prequirúrgico con Albendazol 10 mg/Kg./día durante 7/10 días.
2.2.- PORTADORES NO SINTOMATICOS:
La conducta se decidirá teniendo en cuenta:
- TIPO de Quiste según la Clasificación de Garbhi
- TAMAÑO del Quiste.
Las opciones posibles se presentan en la siguiente Tabla:
Esquema de tratamiento según tipo de quiste y tamaño:
TIPO TAMAÑO CONDUCTA
I MENOR DE 3 CM ELISA. (Ac y Ag)
CONTROL ECOGRAFICO C/ 6 MESES
I DE 3 A 7.5/10 CM TRATAMIENTO CON ALBENDAZOL
I MAYOR DE 7.5/10 CM PUNCION Y/O CIRUGIA
II DE 1 A 7.5/10 CM TRATAMIENTO CON ALBENDAZOL
II MAYOR DE 7.5/10 CM PUNCION Y/O CIRUGIA
III MENOR DE 3CM ELISA (Ac y Ag.)
CONTROL ESTRICTO CADA 3 MESES
III DE 3 A 7.5/10 CM TRATAMIENTO CON ALBENDAZOL
III MAYOR DE 7.5/10 CM PUNCION Y/O CIRUGIA
IV CUALQUIERA EVALUAR SITUACIONES PARTICULARES
HACER DIAGNOSTICO
DIFERENCIAL
CON MASAS HEPATICAS
CONTROL ECOGRAFICO
EVENTUAL TAC, RMN
V CUALQUIERA EVALUAR SITUACIONES PARTICUL.
CONTROL ECOGRAFICO
EVENTUAL TAC, RMN
2.2.1.- TRATAMIENTO CON ALBENDAZOL:
- DOSIS: 10 MG / KG de peso / DIA
En una sola toma diaria luego del desayuno.
Cuatro ciclos de 30 dias cada uno.
Los Ciclos son continuados sin interrupción, excepto intolerancia y/o alteración de los datos del laboratorio. En estos casos se interrumpe por 15 días y se repiten los análisis de Laboratorio. Si se normalizaron los valores alterados se reinicia el tratamiento.
En caso de Intolerancia con síntomas de origen digestivo, se debe asociar con Ranitidina a dosis de 150 mg cada 12 horas vía oral.
- CONTROLES:
a- LABORATORIO: Previo al tratamiento y cada 30 días antes de iniciar cada Ciclo. (Según Ficha de Control de Tratamiento con Albendazol). Se incluirá: Hemograma completo, Urea, creatinina, Coagulogra-ma, Hepatograma completo
b- RADIOLOGIA DE TORAX: Previo al tratamiento.
c- ECOGRAFIA:
A los 2 MESES de inicio del tratamiento.
Al FINALIZAR el tratamiento.
A los 6 meses de finalizado el tratamiento. A los 12 meses de finalizado el tratamiento
d- CLINICO: Evaluar intolerancias, efectos indeseables y/o aparición de síntomas.
- ACCIONES COLATERALES: Puede presentarse disminución de leucocitos, elevación de transaminasas y/o bilirrubina.
- CONTRAINDICACIONES: Embarazo, lactancia, epilepsia, hepatopatía crónica, hipersensibilidad a alguno de sus componentes.
- EVALUACION DEL TRATAMIENTO:
Si durante los controles ecográficos aparecen cambios involutivos del Quiste, ya sea en su tamaño o en su característica, y el paciente persiste asintomático, se debe continuar con controles ecográficos cada 3 a 6 meses para evaluar su evolución.
Si después de pasado el año de finalizado el tratamiento, el paciente persiste asintomático y no hubo ningún tipo de cambio ecográfico del Quiste, se indicará un SE-GÚNDO ESQUEMA DE TRATAMIENTO CON ALBENDAZOL, con las mismas carac-terísticas en cuanto a dosis y controles que el primero.
Aquellos pacientes asintomáticos que por las características del quiste deberían entrar en el Protocolo de Tratamiento con Albendazol, pero:
- No quieren tomar la medicación.
- Presentan intolerancia persistente ya sea clínica o de laboratorio.
- Presentan alguna contraindicación.
Si persisten asintomáticos con quistes hidatídicos menores de 5/7.5 cm de diámetro, entran en protocolo de control y vigilancia ecográfica.
En el caso de quistes de 5 a 10 cm de diámetro, y teniendo en cuenta situaciones particulares de los pacientes, se procederá a indicar otro tipo de tratamiento, como ser Punción y/o Cirugía convencional.
Lo mismo está indicado en aquellos pacientes en los que el tratamiento con Albendazol, luego de los 2 (dos) esquemas propuestos no ha dado resultado, o en aquellos pacientes que se tornan sintomáticos, siempre teniendo en cuenta características individuales de cada paciente.
2.2.2.- TRATAMIENTO MEDIANTE PUNCION.
Se reconoce la utilidad de este método en el tratamiento de la hidatidosis hepática, en pacientes que hayan sido especialmente seleccionados para tal fin.
Se requiere de capacitación específica de los especialistas para la correcta realización del método, a ser aplicado solo en hospitales de complejidad adecuada.
La selección de la técnica de punción a aplicarse debe efectuarse con precaución, dado que en la literatura médica se han descripto situaciones clínicas de complicaciones por el uso de substancias escolicidas intraquísticas.
2.2.3.- TRATAMIENTO POR CIRUGIA CONVENCIONAL:
En caso de estar indicada, se deben aplicar técnicas conservadoras de resección y no deben ser utilizados ningún tipo de escolicidas intraoperatorios.
2.2.4.- TRATAMIENTO POR CIRUGIA LAPAROSCOPICA:
Se recomienda este método solamente para casos debidamente seleccionados, y realizado por un equipo con experiencia previa en cirugía videolaparoscópica.
3 - TRATAMIENTO DE QUISTES HIDATIDICOS ABDOMINALES DE OTRA LOCALIZACION DIFERENTE A LA HEPATICA:
En el caso de quistes hidatídicos intraabdominales no hepáticos, se decide aplicar el mismo criterio que para estos últimos. Siempre teniendo en cuenta las características individuales de cada paciente.
4 - TRATAMIENTO DE QUISTES HIDATIDICOS PULMONARES:
En el caso de PACIENTES SINTOMATICOS se indica la CIRUGIA CONVEN-CIONAL.
En el caso de PACIENTES ASINTOMATICOS, Debe evaluarse cuidadosamente la implementación de otras alternativas de tratamiento, en tanto la eficacia de estos métodos está aún en discusión.
BIBLIOGRAFIA DE REFERENCIA
Arienti H, Guignard S, Rinakldi D, Elbarcha O. Comparison of two serologic methods for the diagnosis of hydatidosis. Rev Panam Salud Publica 5:376-379, 1997
Coltorti E, Fernandez E, Guarnera E, Lago J, Iriarte J. Field Evaluation of an enzyme immunoassay for detection of asymptomatic patients in a hydatid control program. Am J Trop Med Hyg 1988; 38:603-607
Coltorti E. Standarization and evaluation of an Enzime immunoassay as a screening test for the serepidemiology of human Hydatid. Am J Trop Med Hyg 1986; 35:1000-1005
Coltorti E, Varela Diaz V. Detection of antibodies against Echinococcus granulosus arc 5 antigens by double diffusion test. Trans Roy Trop Med Hyg 1978; 72:226-229
Del Carpio M, Moguilansky S, Costa M, Panomarenko H, Bianchi C, Bendersky S, Lazcano Frider B, Larrieu E. Diagnosis of human hydartidosis: predictive value of a rural ultrasonographic survey in an apparently health population. Medicina 2000; 60:466-468
Filice C, Brunetti E. Use of PAIR in human cystic echinococcosis. Proceedings Acta Tropica 1997; 64:95-107
Filice C, Brunetti E, Bruno R, Crippa F. Percutaneus drainage of echinococcal cystic: results of a worldwide survey for assessment of its safety and efficacy. GUT 2000; 47:156-157
Frider B, Losada C, Larrieu E, Zavaleta O. Asymtomatic abdominal hydatidosis detected by ultrasonographia. Acta Radiol 1988; 29:431-434.
Frider B, Larrieu E, Odriozola M. Long term outcome of asymptomatic liver hydatidosis. Hepatology, J Hepatology 1999; 30:228-231
Frider B, Ledesma C, Odriozzola M, Larrieu E. Especificidad de la ecografía en el diagnóstico precoz de la hidatidosis humana. Acta Gastroent Lat Amer 1992; 20:13-15
Frider B, Larrieu E, Aguero A, Catastro ecográfico de Hidatidosis en un área endémica, estudio comparativo con DD5. Rev Iber Parasitol, 1986;46:257-266
Frider B, Larrieu E, Corti O. Frecuencia de las localizaciones hepática y pulmonar del quiste hidatídico en pacientes sintomáticos y en portadores asintomáticos de áreas endémicas. Rev Iber Parasitol 1988; 48:149-153.
Gharby H, Hassine W, Brauner M, Dupuruch K. Ultrasound examination of the hydatic liver. Radiology 1992; 139:459-463
Gil Grande L, Rodríguez Caabeiro F, Prieto J, Sánchez Ruano J, Brasa C, Aguilar L, García F, Casado N, Bárcena R, Alvarez A. Randomised controlled trial of efficacy of albendazol in intra-abdominal hydatid disease. Lancet 1993; 342:1269-1272
Horton R. Albendazole in treatment of human cystic echinococcosis: 12 years of experience. Acta Tropica 1997; 64:79-93
Ivanisevich OR, Rivas C. Equinococcosis Hidatídica, Volume I. Ministerio de Educación and Justice of the Republic Argentina,478 pag, 1961
Khuroo M, Give M, Yatoo S, Zagar S, Javaid G, Khan A, Wedding I. Drenaje percutaneous versus treatment with `albendazole` in liver Hydatidosis: Prospective study. Gastroenterology 1993; 104:1452-1459
Larrieu E. Bases Biológicas y Epidemiológicas para el Control de la Hidatidosis / Equinococcosis. Vet Argentina 1991; 54:612-621
Larrieu E, Guarnera E, Costa M, Alvarez J, Cantoni G, Perez A, Gimenez N. Control de la hidatidosis en la Provincia de Rio Negro. Evaluación actividades atención médica. Rev San Hg Púb. 1993; 5:377-384
Larrieu E, Dapcich C, Guarnera E, Coltorti E, Bianchi C, Moguilansky A. Evaluación de ELISA y DD5 en el diagnóstico de la hidatidosis humana en población asintomática. Rev San Hg Púb 1994; 68:393-398
Larrieu E, Frider B, Andreani G, Andreani G, Aquino A, De La Fuente R. Hidatidosis Humana: ecografía de campo para la determinación de grupos de alto riesgo en la evaluación de un programa de control. Rev Inst trop Sao Paulo. 1989;31:267-270
Larrieu E, Frider B, Del Carpio M, Salvitti J, Mercapide C, Pereyra R, Costa M, Odriozola M, Pe Cantoni G, Sustercic C. Portadores asintomáticos de hidatidosis: epidemiología, diagnóstico y tratamiento. Rev Panamericana de Salud Pública. 2000, in press
Macpherson C, Romig T, Zeyhle E, Rees P, Werw J. Portable Ultrasound scanner versus serology in screening for hydatid cyst in a nomadic population. Lancet 1987; 259-261
Mercapide C, Gimenz R, Pereyra R, Perez C, Michelena F. Tratamiento de la hidatidosis hepática. Pren Méd Argen 1994; 81:275-281
Mlika N, Larouze B, Gaudebout C, Braham B, Allegue M, Dazza M, Dridi M, Gharbi S, Gauner B, Rousset J, Delattre M. Echotomographic and serologic screening for hydatidosis in a Tunisian Village. Am J Trop Med Hyg 1986; 35:815-817
Nahmias J, Goldsmith R, Soibelman M, El On J. Three to 7 year follou up after albendazol treatment of 68 patients with cystic echinococcosis. Ann Trop Med Hyg 1994; 88:295-30335.-
Odriozola M, Pettinari C. Relato Oficial Hidatidosis abdominal. 69 Congreso Argentino de Cirugía. Bs As, 1998
Pelaez V, Kugler C, Del Carpio M. Liver hydatid disease: Results of Percutaneous treatment. Bol Chil Parasitol 1999; 54:63-69
Perdomo R, Parada R, Alvarez C, Cattivelli D, Geninazzi H, Ferreira C, Parada J. Estudio epidemiológico de hidatidosis. Detección precoz por ultrasonido. Rev Med Uruguay 1990; 6:34-47
Perdomo R, Alvarez C, Monti J, Ferreira C, Chiesa A, Carbo A, Alves R, Carmona C, Yarzabal L. Principles of the surgical approach in humzan liver cystic echinococcosis. Acta Tropica 1997; 64:109-122
Saint Martín G, Larrieu E, Chiessa C, Dapcich C. Ultrasound scanning as a screening technique for hydatidosis in developed countries. J Clin Ultrasound 1988; 16:233-237
Salvitti J, Odriozola M, Perez A, Frider B, Larrieu E, Moguilevsky J. Treatment with albendazole of asymptomatic hydatidic carriers. Arch Inter Hid. Vol XXXII, 1997
Schantz P, Williams J, Posse R. Epidemiology of hydatid disease in southern Argentina. Am J Trop Med Hyg 1973;22:629-641
Selentis J, Karpathios T, Fretzayas A, Nicolaidou P, Matsaniotis N. Hydatid disease in asymptomatic young carriers in northern Greece. Am J Trop Med Hyg 1983;32:1462-1463
Shambesh M, Craig P, Gusbi A, Wen H. Immunoblot evaluation of the 100 and 130 Kda antigens camel hydatid cyst fluid for the serodiagnosis of human cystic echinococcosis in Lybia. Trans Royal Soc Trop Med Hyg 1995;89:276-279
Thompson R , Lymbery A. Equinococcus and Hydatid Disease. Ed Cab Internacional (England) 465 pag, 1995
Vagianos C, Karavias D, Kakkos S, Vagenas C, Andoulakis J. Conservative surgery in the tretament of Hepatic Hydatidosis. Eur J Surg 1995; 161:415-420.
WHO informal working group on Echinococcosis. Guidelines for treatment of cystic and alveolar echinococcosis in humans. Bul WHO 1996; 74:231-242
Zamorano C, Contreras M, Sanchez A, Bahamondes M, Sandoval L. Estudio seroepidemiologico de la hidatidosis y triquinosis humana mediante la reaccion de hemaglutinación indirecta en la comuna de San Juan de la Costa, Chile. 1990-1991. Bol Chil Parasitol 1991;46:82-84
ANEXO II
Consejo Provincial de Salud Pública
Comité Provincial de Hidatidosis – Resolución 2688/99
Provincia de Río Negro – República Argentina
Protocolo de Tratamiento / Albendazol
Hospital: Medico Responsable:
Datos del Paciente Nº: H. C. Nº: Edad:
Nombre y Apellido: Lugar:
Fecha de Nacimiento: Anterior:
Domicilio Actual: Ocupación:
ANTECEDENTES PERSONALES DE ENFERMEDAD HIDATIDICA:
Fecha Localización Del Quiste Tratamiento Hospital
...........................................................................................................................................................................
..........................................................................................................................................................................
...........................................................................................................................................................................
ANTECEDENTES FAMILIARES DE ENFERMEDAD HIDATIDICA:
Localización Lugar y Fecha
Nombre y Apellido Edad Parentesco del Quiste del Tratamiento
...........................................................................................................................................................................
...........................................................................................................................................................................
...........................................................................................................................................................................
CONVIVIENTES CON ANTECEDENTES DE ENFERMEDAD HIDATIDICA
Nombre y Apellido Edad Localización Tratamiento
...........................................................................................................................................................................
...........................................................................................................................................................................
...........................................................................................................................................................................
DATOS DE LA ENFERMEDAD ACTUAL:
Localización del Quiste: Diametro:
Características Ecográficas: Tipo (Gharby):
Síntomas: Si – No / Cuales?:
Fecha De Diagnostico:
DATOS PREVIOS Y DURANTE EL TRATAMIENTO:
Fecha de Inicio del Tratamiento: / / . Final del Tratamiento: / / .
Rx de Torax: Fecha. Informe.
Antes del Inicio del Tratamiento
30 DIAS
60 DIAS
90 DIAS
120 DIAS
FECHA
ELISA
PESO KG.
HEMATOCRITO
GLOB. BCOS.
FORMULA
GLUCEMIA
UREMIA
BIL. T/D.
TGO
TGP
FOSF. ALC.
TPO. PROT.
KPTT
PLAQUETAS
PROT. TOT.
ALBUMINA
DOSIS DE ALBENDAZOL
ECOGRAFIAS DE CONTROL:
FECHA
INFORME
DIAMETRO
TIPO (GHARBY)
Efectos Indeseables: (Fecha y Tratamiento)..........................................................................
...........................................................................................................................................................................
ANEXO III
Consejo Provincial De Salud Publica
Programa de Control de la Hidatidosis
Provincia de Río Negro. Ficha Individual – Catastro Ecográfico
Datos Personales:
Apellido y Nombre: .......................................................................................................................Edad:................
Sexo: M / F ....... Fecha y Lugar de Nacimiento: ...............................................................
Domicilio: ..............................................................................ESCUELA Nº ..................................
Antecedentes de Enfermedad Hidatídica:
Fecha Tipo de Quiste Parentesco
Personales: Si / No
Familiares: Si / No
Datos Actuales:
Sintomas: Si / No (Cuales:.........................................................)
Rx de Torax: Si / No Normal / Patología
Laboratorio: Si / No Elisa / Otros...................................................
Ecografía: Normal / Patología
Localización Tamaño Tipo Características
Datos Del ......................................................................................................
Quiste
...............................................................................................................................
Standards for Diagnosis and Treatment of Human Echinococcosis
DIAGNOSIS AND TREATMENT STANDARDS OF HUMAN HIDATIDOSIS
Río Negro PROVINCE (ARGENTINA)
RESOLUTION 3720/2002. SECRETARY OF HEALTH
Design and Drafting Group:
In alphabetical order:
Dr. Mario Del Carpio (Surgeon), Hopital R. Cortizo, Ing. Jacobacci
Dr. Antonio Gatti (Bioquimico), Hospital A. Zatti, Viedma.
Dr. Carlos Hugo Mercapide (Head of Surgery), Hospital A. Zatti, Viedma.
Dr. Martin Odriozola (Head of Surgery) Hospital R. Carrillo, Bariloche.
Dr. Hector Panomarenko (Generalist Medical) Area Hospital, El Bolson
Dr. Rubén Pereyra (Surgeon), Hospital A. Zatti, Viedma.
Dr. Alicia Perez (Biochemistry). Laboratory of Zoonosis, Bariloche
Dr. Juan Carlos Salvitti (Surgeon), Hospital Carrillo, Bariloche
Dr. José Sustersic (Surgeon), Hospital Lopez Lima, Rock.
.
Technical Assistance (veterinarians)
Dra. Maria Teresa Costa, Regional Epidemiology Unit, Jacobacci
Dr. Gustavo Cantoni, Regional Epidemiology Unit, Bariloche
Dr. Jose Labanchi, Regional Epidemiology Unit, Rock
Dr. Sergio Mancini, Regional Epidemiology Unit, Viedma
Dr. Ricardo Bigatti, Hydatid Control Program, Ministry of Health
General coordination
Dr. Edmundo Larrieu (veterinarian), Priority Areas Directorate, Ministry of Salud
ANEXO I
RULES OF DIAGNOSIS AND TREATMENT
HUMAN HIDATIDOSIS
INTRODUCTION: EPIDEMIOLOGICAL BASIS FOR THE DIAGNOSIS AND TREATMENT OF HUMAN HIDATIDOSIS
The Echinococcus granulosus in its adult form lives in the intestine of the dog, removing eggs regularly with the stool. These eggs can be accidentally ingested by intermediate hosts, including humans. The eggs hatch, releasing hexacanto embryo into the small intestine. This, through the villi passes the venous circulation to stay in liver tissue where hydatid form. At 72 hours after ingestion of egg, larva reaches a size of 20 microns, whereas at 7 days can identify a spherical and frankly hydatid training.
Should be overcome liver filter the embryo continues through the circulatory system to the lung. Can continue their migration eventually reaching various locations such as kidney, brain, bone, muscle, etc.
Parasite growth depend on the evolutionary potential of hexacanto embryo surrounding tissue and host resistance.
Thus, the lung, elastic characteristics, provides little resistance to growth. This determines an increase in size proportionally faster leading to clinical symptoms in a large percentage of cases.
In the liver, meanwhile, the resistance of the surrounding tissue is strong that determines that in many cases the growth is slow or even zero for many years, allowing a high percentage of carriers remain without clinical symptoms throughout their lives.
These features translate into a relationship between locations liver / lung 2/1 to 3/1 in hospital receiving patients with clinical symptoms. The remaining locations usually do not exceed 10% of detected cases. These coefficients expressing the importance of liver filter as the location determining element cyst.
The autopsy studies, meanwhile, show a relationship between lung and liver locations where 4/1 and between 63.3% and 84.5% of cases result from findings unrelated to the cause of death. This figure reinforces the filter criteria in the liver as the primary factor in determining location and expresses that a significant percentage of hepatic cysts reaches not produce disease in the host, maintaining a state of agent / host balance throughout life.
1- DIAGNOSIS OF HIDATIDOSIS IN MAN:
1.1 DIAGNOSTIC IMAGING:
1.1.1 HIDATIDOSIS LIVER AND ABDOMINAL: Consideration should be given to the ultrasound technique of choice for:
a- diagnosis in symptomatic patients.
b- Control treatment
c- population surveys to detect non-symptomatic abdominal (90% of hydatid cysts) location carriers. In these cases the technique sensitivity is 100% and the specificity 96%.
d- Surveillance.
From the point of view of the ultrasound images of hydatid cyst, defined several pathognomonic features:
a.- isolated vesicles.
b.- multiple daughter cysts.
c.- observation of "snow" given by the mobilization of the hydatid sand to mobilize the patient abruptly 180 degrees.
d.- sloughed appearance of membranes.
e.- hydatid cyst wall thicker (difference with simple serous cysts or polycystic disease).
The ultrasonographic diagnosis should include Gharby classification (type of cyst):
TYPE I: Hyaline
TYPE II: Membranes "folded"
TYPE III: With vesicles Daughters
TYPE IV: Solid Heterogeneous
TYPE V: Calcified
In all cases the correct measurement of the size and location of the cyst ultrasound, essential elements for therapeutic decision and for the control and monitoring of patients will be included.
Other diagnostic imaging methods (CT - NMR) are reserved for selected and / or ultrasound doubtful cases.
The residences in General Medicine should include training in ultrasound field in its curriculum.
1.1.2 HIDATIDOSIS PULMONARY should be considered a chest radiograph (front and profile) technique of choice for:
a- diagnosis in symptomatic patients
b- Control treatment
c- population surveys to detect non-symptomatic lung (10% of hydatid cysts) location carriers.
1.2 LABORATORY DIAGNOSIS:
1.2.1 ELISA (antibodies): Useful as sieve technique for detection surveys village-res non-symptomatic, particularly in the absence of ultrasound technology.
1.2.2 ELISA (circulating antigen) or capture Elisa. Useful for monitoring patients operated and / or treatment with albendazole. The first determination should be performed before surgery or treatment was started.
Controls should be performed at 10 and 30 days after surgery, at 3 months and then every 6 months. Normally 30 days it becomes negative.
For patients under medical treatment, be performed every 3-6 months determinations.
In symptomatic patients with surgically confirmed hydatid disease has been reported that 80% of cases with a positive serology for indirect hemagglutination, 82% to 88% for double diffusion five 82% for immunoelectrophoresis, 88% to 96% for enzyme immunoassay, and 92% for immunoblotting. The specificity of these methods ranges from 95% to 100% HAI DD5.
In patients without clinical symptoms information is very limited, although the serological response is markedly lower.
For example, the sensitivity and specificity of double diffusion tests five enzyme immunoassay have been estimated in the Province of Rio Black using complete imaging (radiology, ultrasonography and CT) as benchmarks, resulting in 63% and 97.05% studies Enzyme immunoassay respectively equal to or greater than 8, titles, and 31% and 100% respectively for DD5. Accordingly:
- DD5: its use is not recommended for low sensitivity and high consumption of antigen.
- HAI: its use is not recommended for filing false positives and false negatives. Its sensitivity and specificity are less than ELISA.
In all cases the negativity of a serological test can not rule out the presence of a hydatid cyst in both healthy carriers as symptomatic patients.
1.3.- POPULATION SURVEY
Its low operating cost, speed of obtaining results, high diagnostic yield and accuracy of the result (positive predictive value present in the Province of Rio Black 20%, negative predictive value 100%) place ultrasonographic survey as a method of choice in the diagnosis early human hydatid disease in endemic areas.
However, this is not available ultrasound equipment for routine use in endemic rural settings, could be used enzyme immunoassay as a screening test being reactive cases referred for more complex centers to be studied with abdominal ultrasonography and eventually pulmonary radiology .
2- TREATMENT OF LIVER CYST hydatid:
Suggestions treatment detailed below are based on experience so far gained in the development of program control and treatment of these patients and are for general guidance, the physician must consider individually each patient to to identify and evaluate those particular situations (such as age, previous illnesses, specific contraindications, occupation, address, chances of making the necessary controls, etc.) that may make it necessary to tailor treatment to the individual patient conditions. If in doubt suggested communicate the Provincial Medical Committee and / or regional benchmarks.
One must consider two situations:
a) .- Symptomatic patients and / or complicated hydatid cysts
b) .- asymptomatic carriers of hydatid cysts.
Must properly assess the symptoms reported by the patient to determine if they are really caused by hydatid cyst or are caused by other illness.
All patients is owed, plus ultrasonography, chest radiology make before deciding what action to take.
2.1 symptomatic patients and / or COMPLICATED:
Either by infection, ruptured abdominal cavity or the biliary tract, chest and abdomen, transit or palpable tumor is suggested SURGICAL TREATMENT convinced-NAL.
Preoperative treatment in such cases be made with Albendazole 10 mg / kg. / Day for 7-10 days.
NO CARRIER 2.2 symptomatic:
The behavior will be decided taking into account:
- TYPE cyst according to the Classification of Garbhi
- SIZE cyst.
The options are presented in the following Table:
Treatment schedule by type of cyst and size:
TYPE SIZE CONDUCT
I LESS THAN 3 CM ELISA. (Ac and Ag)
ULTRASONOGRAPHIC CONTROL C / 6 MONTHS
I 3 TO 7.5 / 10 CM albendazol
I OVER 7.5 / 10 CM PUNCTURE AND / OR SURGERY
II 1 TO 7.5 / 10 CM albendazol
SENIOR II 7.5 / 10 CM PUNCTURE AND / OR SURGERY
UNDER III ELISA 3CM (Ac and Ag.)
STRICT CONTROL EVERY 3 MONTHS
III 3 TO 7.5 / 10 CM albendazol
SENIOR III 7.5 / 10 CM PUNCTURE AND / OR SURGERY
IV EVALUATE ANY PARTICULAR SITUATIONS
DO DIAGNOSIS
DIFFERENTIAL
MASS WITH LIVER
ULTRASONOGRAPHIC CONTROL
POSSIBLE CT, MRI
EVALUATE ANY SITUATIONS V by owner.
ULTRASONOGRAPHIC CONTROL
POSSIBLE CT, MRI
2.2.1 TREATMENT ALBENDAZOLE:
- DOSE: 10 MG / KG weight / DIA
At once daily after breakfast.
Four cycles of 30 days each.
The cycles are continued without interruption, except intolerance and / or alteration of the laboratory data. In these cases it is interrupted for 15 days and laboratory tests are repeated. If the altered values were normalized treatment is restarted.
In case of intolerance with symptoms of gastrointestinal origin, must be associated with ranitidine at a dose of 150 mg orally every 12 hours.
- CONTROLS:
a- LABORATORY: Prior to treatment and every 30 days before each cycle. (According Tab Control Treatment with albendazole). It will include: Complete blood count, urea, creatinine, Coagulogra-ma, hepatograma full
b- chest radiography: Prior to treatment.
c- ECOGRAFIA:
At 2 months of starting treatment.
Al END treatment.
At 6 months after treatment completion. At 12 months after treatment completion
d- CLINIC: Evaluate intolerances, side effects and / or appearance of symptoms.
- SIDE ACTION: decreased leukocytes may occur, elevated transaminases and / or bilirubin.
- Contraindications Pregnancy, breastfeeding, epilepsy, chronic liver disease, hypersensitivity to any of its components.
- EVALUATION OF TREATMENT:
If during the ultrasound controls are involutive changes cyst, either in size or their property, and the patient remains asymptomatic, continue with ultrasound scans every 3-6 months to evaluate your progress.
If last year after the end of treatment, the patient remains asymptomatic and there was any change cyst ultrasound, indicate a SE-second TREATMENT SCHEME ALBENDAZOLE, with the same charac-teristics in terms of dose and controls than the former.
Those asymptomatic patients by the characteristics of the cyst should enter the Protocol Treatment with albendazole, but:
- Do not want to take medication.
- Present persistent intolerance either clinical or laboratory.
- They have a contraindication.
If hydatid cysts remain asymptomatic with under 5 / 7.5 cm in diameter, enter control protocol and ultrasound surveillance.
For cysts of 5-10 cm in diameter, and taking into account particular situations of patients will proceed to indicate another type of treatment, such as puncture and / or conventional surgery.
The same is indicated in those patients in whom treatment with albendazole, after 2 (two) proposed schemes has not worked, or in patients who become symptomatic, taking into account individual characteristics of each patient.
2.2.2 TREATMENT WITH PUNCTURE.
The usefulness of this method in the treatment of hepatic hydatid disease is recognized, in patients who have been specially selected for this purpose.
It requires specific training of specialists for the correct application of the method to be applied only in hospitals adequate complexity.
Selecting the puncture technique applied must be made with caution, since in the literature have described clinical situations of complications from the use of substances intracyst escolicidas.
2.2.3 CONVENTIONAL TREATMENT FOR SURGERY:
Should be indicated, should be applied conservative resection techniques and should not be used any intraoperative escolicidas.
2.2.4 TREATMENT BY LAPAROSCOPIC SURGERY:
This method is recommended only for properly selected cases, and conducted by a team with previous experience in laparoscopic surgery.
3 - TREATMENT OF ABDOMINAL hydatid Cysts A DIFFERENT LOCATION TO THE LIVER:
In the case of non-hepatic intra-abdominal hydatid cysts, it was decided to apply the same criteria as for the latter. Always considering the individual characteristics of each patient.
4 - TREATMENT OF LUNG Hydatid Cysts:
For symptomatic patients SURGERY CONVEN-TIONAL indicated.
For asymptomatic patients, the implementation of other treatment options should be carefully evaluated, while the effectiveness of these methods is still under discussion.
BIBLIOGRAPHY OF REFERENCE
Arienti F, S Guignard, Rinakldi D, Elbarcha O. Comparison of two methods for the serologic diagnosis of hydatidosis. Rev Panam Salud Publica 5: 376-379, 1997
Coltorti E, Fernandez E, Guarnera E, Lake J, J. Iriarte Field Evaluation of an enzyme immunoassay for detection of asymptomatic patients in a hydatid monitoring program. Am J Trop Med Hyg 1988; 38: 603-607
Coltorti E. Standardization and evaluation of an Enzyme immunoassay as a screening test for the serepidemiology of human Hydatid. Am J Trop Med Hyg 1986; 35: 1000-1005
Coltorti E, Diaz Varela V. Detection of antibodies Against Echinococcus granulosus arc five antigens by double diffusion test. Trop Med Hyg Trans Roy 1978; 72: 226-229
Del Carpio M, Moguilansky S, Costa M, Panomarenko M, Bianchi C, Bendersky S, Lazcano Frider B, Larrieu E. Diagnosis of human hydartidosis: predictive value of a rural ultrasonographic survey in an Apparently population health. Medicine 2000; 60: 466-468
Filice C, Brunetti E. Use of human cystic echinococcosis in PAIR. Acta Tropica Proceedings 1997; 64: 95-107
Filice C, Brunetti E, Bruno R, F. Crippa Percutaneus drainage of cystic echinococcal: results of a worldwide survey for assessment of safety and efficacy STIs. GUT 2000; 47: 156-157
Frider B, C Losada, Larrieu E, Zavaleta O. Asymtomatic detected by abdominal hydatidosis ultrasonographia. Acta Radiol 1988; 29: 431-434.
Frider B, Larrieu E, Odriozola M. Long term outcome of asymptomatic liver hydatidosis. Hepatology, J Hepatology 1999; 30: 228-231
Frider B, C Ledesma, Odriozzola M, Larrieu E. Specificity of ultrasound in early diagnosis of human hydatidosis. Lat Amer Gastroent Act 1992; 20: 13-15
Frider B, Larrieu E, Aguero A, ultrasound Cadastre Hidatidosis in an endemic area, comparative study with DD5. Rev Iber Parasitol 1986; 46: 257-266
Frider B, Larrieu E, O. Corti locations Frequency of hepatic and pulmonary hydatid cyst in symptomatic patients and asymptomatic carriers of endemic areas. Rev. Iber Parasitol 1988; 48: 149-153.
Gharby H, Hassine W, Brauner M, Dupuruch K. hydatic Ultrasound examination of the liver. Radiology 1992; 139: 459-463
Large Gil L, Rodríguez Caabeiro F, Prieto J, Sánchez Ruano J, Brasa C, Aguilar L, García F, Married N, Barcena R, Alvarez A. Randomised controlled trial of efficacy of albendazole in intra-abdominal hydatid disease. Lancet 1993; 342: 1269-1272
R. Horton Albendazole in treatment of human cystic echinococcosis: 12 years of experience. Tropica Acta 1997; 64: 79-93
Ivanisevich OR, C. Rivas hydatid echinococcosis, Volume I. Ministry of Education and Justice of the Republic Argentina, 478 pp, 1961
Khuroo M, Give M, YATOO S, S Zagar, Javaid G, Khan A, Wedding versus percutaneous drainage treatment I. With `albendazole` in liver hydatidosis: Prospective study. Gastroenterology 1993; 104: 1452-1459
Larrieu E. Bases Biological and Epidemiological Control hydatidosis / echinococcosis. Argentina Vet 1991; 54: 612-621
Larrieu E, Guarnera E, Costa M, Alvarez J, Cantoni G, Perez A, Gimenez N. Control of hydatid disease in the Province of Rio Black. Evaluation health care activities. Rev San Hg Pub. 1993; 5: 377-384
Larrieu E, Dapcich C, Guarnera E, Coltorti E, Bianchi C, Moguilansky A. Evaluation of ELISA and DD5 in the diagnosis of human hydatid disease in asymptomatic population. San Hg Púb Rev 1994; 68: 393-398
Larrieu E, Frider B, Andreani G, G Andreani, Aquino A, De La Fuente R. Hidatidosis Humana: ultrasound field for determining high-risk groups in the evaluation of a control program. Rev Inst trop Sao Paulo. 1989; 31: 267-270
Larrieu E, Frider B, Del Carpio M, Salvitti J, Mercapide C, Pereyra R, Costa M, Odriozola M, G Pe Cantoni, C. Sustercic asymptomatic carriers of hydatid disease: epidemiology, diagnosis and treatment. Pan Rev Public Health. 2000, in press
Macpherson C, Romig T, Zeyhle E, P Rees, J. werw Portable Ultrasound scanner versus serology in screening for hydatid cyst in a nomadic population. Lancet 1987; 259-261
Mercapide C, Gimenz R, Pereyra R, Perez C, Michelena F. Treatment of hepatic hydatid disease. Pren Argen Med 1994; 81: 275-281
Mlika N, Larouze B, C Gaudebout, Braham B, Allegue M, Dazza M, M Dridi, Gharbi S, Gauner B, Rousset J, Delattre M. Echotomographic and serologic screening for hydatidosis in a Tunisian Village. Am J Trop Med Hyg 1986; 35: 815-817
Nahmias J, Goldsmith R, Soibelman M, The Three J. On follou up to 7 year after albendazole treatment of 68 patients With cystic echinococcosis. Ann Trop Med Hyg 1994; 88: 295-30335.-
Odriozola M, Pettinari C. Story Official abdominal hydatidosis. 69 Argentine Congress of Surgery. Buenos Aires, 1998
Pelaez V, Kugler C, Del Carpio M. Liver hydatid disease: Results of Percutaneous treatment. Bol Chil Parasitol 1999; 54: 63-69
Perdomo R, Parada R, Alvarez C, D Cattivelli, Geninazzi H, Ferreira C, Parada J. Epidemiology of hydatid disease. Early detection by ultrasound. Rev Med Uruguay 1990; 6: 34-47
Perdomo R, Alvarez C, Monti J, Ferreira C, Chiesa A, Carbo A, Alves R, Carmona C, Yarzábal L. Principles of the surgical approach in humzan liver cystic echinococcosis. Tropica Acta 1997; 64: 109-122
Saint Martin G, Larrieu E, Chiessa C, Dapcich C. Ultrasound scanning as a screening technique for hydatidosis in developed country clubs. J Clin Ultrasound 1988; 16: 233-237
Salvitti J, Odriozola M, Perez A, B Frider, Larrieu E, Moguilevsky J. Treatment of asymptomatic albendazole With hydatidic carriers. Arch Inter Hid. Vol XXXII, 1997
Schantz P, Williams J, Posse R. Epidemiology of hydatid disease in southern Argentina. Am J Trop Med Hyg 1973; 22: 629-641
Selentis J, Karpathios T, Fretzayas A, Nicolaidou P, N. Matsaniotis Hydatid disease in young asymptomatic carriers in northern Greece. Am J Trop Med Hyg 1983; 32: 1462-1463
Shambesh M, Craig P, Gusbi A, Wen H. Immunoblot evaluation of the 100 and 130 kDa hydatid cyst fluid camel antigens for the serodiagnosis of human cystic echinococcosis in Lybia. Trans Royal Soc Trop Med Hyg 1995; 89: 276-279
Thompson R, Lymbery A. Echinococcus and Hydatid Disease. Ed Cab International (England) 465 pp, 1995
Vagianos C, D Karavias, Kakkos S, Vagenas C, Andoulakis J. Conservative surgery in the tretament of Hepatic hydatidosis. Eur J Surg 1995; 161: 415-420.
WHO Informal working group on Echinococcosis. Guidelines for treatment of cystic and alveolar echinococcosis in humans. Bul WHO 1996; 74: 231-242
Zamorano C, Contreras M, Sanchez A, Bahamondes M, L. Sandoval seroepidemiological study of human hydatidosis and trichinosis by indirect hemagglutination reaction in the municipality of San Juan de la Costa, Chile. 1990/1991. Bol Chil Parasitol 1991; 46: 82-84
ANNEX II
Provincial Public Health Council
Provincial Committee Hidatidosis - Resolution 2688/99
Black River Province - Argentina Republic
Treatment Protocol / Albendazole
Hospital Medical Responsible:
Patient Data NO: H. C. NO: Age:
Name: Location:
Date of Birth: Previous:
Current Address: Occupation:
PERSONAL HISTORY hydatid disease:
Date Location Cyst Treatment Hospital
...........................................................................................................................................................................
..........................................................................................................................................................................
...........................................................................................................................................................................
FAMILY HISTORY OF hydatid disease:
Location Location and Date
Full Name Age Relationship Cyst Treatment
...........................................................................................................................................................................
...........................................................................................................................................................................
...........................................................................................................................................................................
BACKGROUND having lived with hydatid disease
Your Name Age Location Treatment
...........................................................................................................................................................................
...........................................................................................................................................................................
...........................................................................................................................................................................
DATA PRESENT ILLNESS:
Cyst Location: Diameter:
Sonographic features: Type (Gharby):
Symptoms: Yes - No / What ?:
Date Diagnosis:
BACKGROUND AND DATA DURING TREATMENT:
Treatment Start Date: / /. End of Treatment: / /.
CXR: Date. Report.
Before the Start of Treatment
30 DAYS
60 DAYS
90 DAYS
120 DAYS
DATE
ELISA
WEIGHT KG.
HEMATOCRITO
GLOB. BCOS.
FORMULA
GLUCEMIA
UREMIA
BIL. T / D.
TGO
TGP
Alk. ALC.
TPO. PROT.
KPTT
PLAQUETAS
PROT. TOT.
ALBUMINA
DOSE ALBENDAZOLE
Ultrasound CONTROL:
DATE
REPORT
DIAMETER
TYPE (Gharby)
Undesirable effects: (Date and Treatment) .......................................... ................................
...........................................................................................................................................................................
ANNEX III
Provincial Public Health Council
Control Program Hydatidosis
Black River Province. Single Sheet - Cadastral Ecographic
Personal Data:
Name and Surname:.......................................................................................................................Edad:................
Gender: M / F ....... Date and Place of Birth: ................................ ...............................
Address: ................................................ NO SCHOOL .............................. .................. ................
Background of hydatid disease:
Date Type of cyst Relationship
Personal: Yes / No
Family: Yes / No
Current data:
Symptoms: Yes / No (What: .......................................... ...............)
CXR: Yes / No Normal / Pathology
Lab: Yes / No Elisa / Other .......................................... .........
Ultrasound: Normal / Pathology
Location Size Type Features
DETAIL......................................................................................................
cyst
...............................................................................................................................
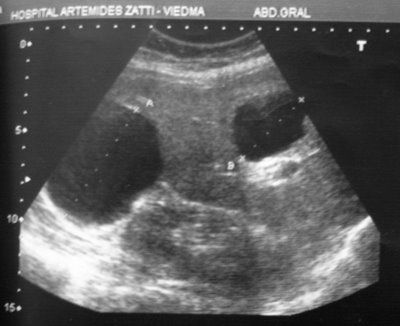
 Tipo II. Membrana "plegada" (desprendida) Es característico de los quistes hidatídico hepático, se observa el deprendimiento de la membrana germinativa. Puede haber también plegamientos de la misma. Los > a 7-10 cm son quirúrgicos, los < los tratamos con Albendazol.
Tipo II. Membrana "plegada" (desprendida) Es característico de los quistes hidatídico hepático, se observa el deprendimiento de la membrana germinativa. Puede haber también plegamientos de la misma. Los > a 7-10 cm son quirúrgicos, los < los tratamos con Albendazol. Tipo III. Multivesicular. Se observan múltiples vesículas hijas que le dan el aspecto característico de panal de abejas. Los de > 7-10 cm son quirúrgicos. Son los más agresivos y tienden a complicarse por ejemplo abriéndose a la vía biliar. Los < los tratamos con Albendazol.
Tipo III. Multivesicular. Se observan múltiples vesículas hijas que le dan el aspecto característico de panal de abejas. Los de > 7-10 cm son quirúrgicos. Son los más agresivos y tienden a complicarse por ejemplo abriéndose a la vía biliar. Los < los tratamos con Albendazol. Tipo IV. Sólido heterogéneo. Inactivo. Corresponde a la "papilla o puré" hidatídica compuesto por membranas inactivas y material necrótico. Tienen un mínimo componente líquido por lo que tiene un leve refuerzo posterior. Debe hacerse diagnóstico diferencial con tumores hepáticos secundarios (metástasis). En general no requieren tratamiento y debe hacerse un seguimiento ecográfico cada 6 meses mientras sea asintomático.
Tipo IV. Sólido heterogéneo. Inactivo. Corresponde a la "papilla o puré" hidatídica compuesto por membranas inactivas y material necrótico. Tienen un mínimo componente líquido por lo que tiene un leve refuerzo posterior. Debe hacerse diagnóstico diferencial con tumores hepáticos secundarios (metástasis). En general no requieren tratamiento y debe hacerse un seguimiento ecográfico cada 6 meses mientras sea asintomático. Tipo V. Calcificado. Inactivo. El ultrasonido se refleja por completo en el quiste calcificado y por ello se ve blanco y al no poder atravesarlo deja una sombra "acústica" negra por detrás del mismo. Son quistes "muertos" y no requieren de ningún tipo de tratamiento ni control.
Tipo V. Calcificado. Inactivo. El ultrasonido se refleja por completo en el quiste calcificado y por ello se ve blanco y al no poder atravesarlo deja una sombra "acústica" negra por detrás del mismo. Son quistes "muertos" y no requieren de ningún tipo de tratamiento ni control.